Leçon 2 : L’atome et les ions
I. L’atome
1. Constituants de l’atome
L’atome est constitué :
- d’un noyau chargé positivement,
- d’électrons chargés négativement qui gravitent autour.
2. Modèles de l’atome
a) Ancien modèle (Bohr)Dans ce modèle, les électrons tournent autour du noyau sur des trajectoires circulaires appelées “orbites”.
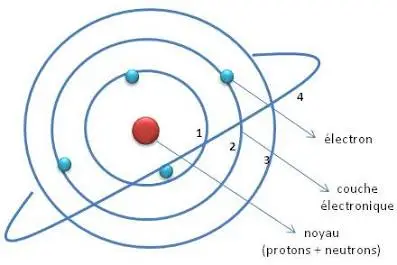 b) Modèle actuel (Schrödinger)
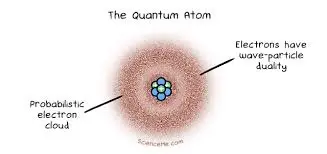
b) Modèle actuel (Schrödinger)
Les électrons ne suivent pas d’orbites précises : ils forment un nuage électronique autour du noyau.
3. Le noyau
- Situé au centre de l’atome.
- Porte les charges positives (protons).
- Contient presque toute la masse de l’atome.
- Son diamètre est environ 100 000 fois plus petit que celui de l’atome.
4. Les électrons
- Très légers et en mouvement rapide.
- Ils forment le nuage électronique.
- Charge d’un électron : – e.
- Valeur de la charge élémentaire : e = 1,6 × 10⁻¹⁹ C.
- Les électrons sont identiques quel que soit l’atome.
Remarque : Chaque atome possède un nombre bien déterminé d’électrons.
II. Neutralité électrique de l’atome
Un atome est électriquement neutre :
il possède autant de charges positives (protons) que de charges négatives (électrons).
1. Le numéro atomique (Z)
Z est le nombre de protons (charges positives du noyau).
Comme l’atome est neutre :
Z = nombre de protons = nombre d’électrons.
Exemple : Lithium → Z = 3 → noyau = 3 protons → 3 électrons.
2. Charge électrique de l’atome
Charge du noyau : + Z·e
Charge totale des électrons : – Z·e
Donc : (+ Z·e) + (– Z·e) = 0
➡️ L’atome est neutre.
Charge totale des électrons : – Z·e
Donc : (+ Z·e) + (– Z·e) = 0
➡️ L’atome est neutre.
III. Les ions
1. Définition
Un ion est un atome (ou un groupe d’atomes) qui a perdu ou gagné des électrons.
2. Ions monoatomiques
a) Le cation (ion positif)
Un atome qui perd un ou plusieurs électrons devient un ion positif (cation).
Exemple : Li → Li⁺ (perd 1 électron)
Un atome qui gagne un ou plusieurs électrons devient un ion négatif (anion).
Exemple : Cl → Cl⁻ (gagne 1 électron)
3. Les ions polyatomiques
| Ion | Formule | Charge |
|---|---|---|
| Hydroxyde | OH⁻ | –e |
| Nitrate | NO₃⁻ | –e |
| Sulfate | SO₄²⁻ | –2e |
| Ammonium | NH₄⁺ | +e |
Remarque : Les solutions aqueuses sont conductrices grâce aux ions.