Leçon : Réactions des solutions d’acide avec quelques métaux
I. Réactions d’une solution d’acide chlorhydrique avec des métaux
a. Expérience
On place dans quatre tubes : du cuivre (Cu), du fer (Fe), de l’aluminium (Al) et du zinc (Zn). On ajoute une solution d’acide chlorhydrique (H⁺ + Cl⁻).
On approche ensuite une flamme à l’ouverture de chaque tube.
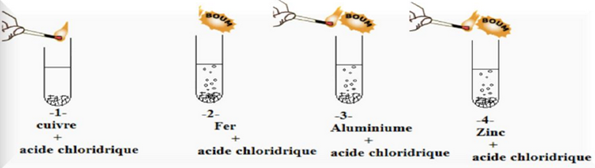
b. Résultats
- L’acide chlorhydrique réagit avec tous les métaux sauf le cuivre.
- Une détonation (petite explosion sonore) se produit dans les tubes contenant Fe, Al et Zn.
- Le tube contenant le fer devient vert à la fin de la réaction.
c. Interprétation
- Le gaz qui produit la détonation est le dihydrogène H₂.
- La couleur verte indique la présence des ions fer II (Fe²⁺).
- Les métaux Fe, Al et Zn disparaissent peu à peu car ils se transforment en ions : Fe → Fe²⁺, Al → Al³⁺, Zn → Zn²⁺.
d. Conclusion
✔ Le fer, le zinc et l’aluminium réagissent et produisent : dihydrogène (H₂) + ions métalliques (Fe²⁺, Al³⁺, Zn²⁺).
e. Équations chimiques des réactions
1. Fer + acide chlorhydrique
Bilan : Fer + acide chlorhydrique → dihydrogène + chlorure de fer II
Équation : Fe + 2(H⁺ + Cl⁻) → H₂ + (Fe²⁺ + 2Cl⁻)
Simplifiée : Fe + 2H⁺ → H₂ + Fe²⁺
2. Aluminium + acide chlorhydrique
Bilan : Aluminium + acide chlorhydrique → dihydrogène + chlorure d’aluminium
Équation : 2Al + 6(H⁺ + Cl⁻) → 3H₂ + (2Al³⁺ + 6Cl⁻)
Simplifiée : 2Al + 6H⁺ → 3H₂ + 2Al³⁺
3. Zinc + acide chlorhydrique
Bilan : Zinc + acide chlorhydrique → dihydrogène + chlorure de zinc
Équation : Zn + 2(H⁺ + Cl⁻) → H₂ + (Zn²⁺ + 2Cl⁻)
Simplifiée : Zn + 2H⁺ → H₂ + Zn²⁺
II. Réaction d’une solution de soude avec quelques métaux
1. Expérience
On place dans quatre tubes à essai les métaux suivants : cuivre (Cu), fer (Fe), aluminium (Al) et zinc (Zn). On ajoute une solution de soude (Na⁺ + OH⁻) dans chaque tube.
Image : Métaux + solution de soude (Cu, Fe, Al, Zn)
Ensuite, on approche une flamme à l’ouverture de chaque tube.
2. Observation
- Le cuivre (Cu) : aucune réaction visible.
- Le fer (Fe) :aucune réaction visible. .
- L’aluminium (Al) : réaction forte, dégagement important de gaz.
- Le zinc (Zn) : réaction plus lente, dégagement de gaz.
- Lorsque la flamme est approchée des tubes contenant Al et Zn, on observe une détonation.
3. Conclusion
✔ L’aluminium et le zinc réagissent fortement avec la soude.
✔ Cette réaction produit un gaz inflammable : dihydrogène (H₂).
✔ Le métal (Al ou Zn) disparaît peu à peu car il se transforme en ions métalliques.